Prospective phase II trial of regional hyperthermia and whole liver irradiation for numerous chemorefractory liver metastases from colorectal cancer
Radiation oncology journal. 2016 Mar; vol. 34,1, 34–44.
Jeong Il Yu, MD1, Hee Chul Park, MD, PhD1,2, Doo Ho Choi, MD, PhD1, Jae Myoung Noh, MD1, Dongryul Oh, MD1, Jun Su Park, MD1, Ji Hyun Chang, MD3, Seung Tae Kim, MD4, Jeeyun Lee, MD, PhD4, Se Hoon Park, MD4, Joon Oh Park, MD4, Young Suk Park, MD4, Ho Yeong Lim, MD, PhD4, Won Ki Kang, MD4
- Department of Radiation Oncology, Samsung Medical Center, Sungkyunkwan University School of Medicine, Seoul, Korea.
- Department of Medical Device Management and Research, Samsung Advanced Institute for Health Sciences and Technology,
- Sungkyunkwan University, Seoul, Korea.
- Department of Radiation Oncology, Seoul St. Mary's Hospital, The Catholic University of Korea College of Medicine, Seoul, Korea.
- Department of Medicine, Samsung Medical Center, Sungkyunkwan University School of Medicine, Seoul, Korea.
תקציר
מטרת המחקר– נערך ניסוי פאזה 2 פרוספקטיבי, על מנת להעריך את היעילות והרעילות של היפרתרמיה אזורית (regional hyperthermia) וטיפול קרינתי לכל הכבד (whole liver irradiation) עבור גרורות מרובות בכבד, שמקורן מסרטן המעי הגס (colorectal cancer) אשר עמידות לכימותרפיה (chemorefractory hepatic metastases).
חומרים ושיטות– למטופלים שגויסו היו עבור גרורות מרובות בכבד, שמקורן מסרטן המעי הגס אשר עמידות לכימותרפיה. תוכננו חמישה מפגשי טיפול של היפרתרמיה ושבעה פרקציות ב-3 Gy של טיפול קרינתי לכל הכבד (WLI). איכות חיים הקשורה לבריאות (Health-related quality of life) נקבעה באמצעות הגרסה הקוריאנית של שאלון איכות החיים של הארגון האירופי לחקר וטיפול בסרטן C-30 (European Organization for Research and Treatment of Cancer quality of life questionnaire ) וההערכה הפונקציונאלית של טיפול בסרטן–הכבד ודרכי המרה גרסה 4.0 (Functional Assessment of Cancer Therapy-Hepatobiliary). הוערכה תגובה אובייקטיבית ותגובת כאב.
תוצאות – סך של 12 מטופלים הסכימו למחקר ול-10 מטופלים שקיבלו טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה בוצעה אנליזה. טיפול קרינתי לכל הכבד (WLI) הושלם כמתוכנן בתשעה מטופלים והיפרתרמיה בשמונה מטופלים. תגובת הכאב (Pain response) הייתה חלקית (partial) בארבעה מטופלים ויציבה (stable) אצל ארבעה. תגובה אובייקטיבית חלקית (Partial objective response) הושגה בשלושה מטופלים (30.0%) ומחלה יציבה (stable disease) נצפתה בארבעה מטופלים במעקב של חודש אחד. מטופל אחד נפטר חודש לאחר הטיפול בגלל אי ספיקה נשימתית הקשורה להתקדמות של גרורות פלאורליות (pleural metastasis). רעילויות אחרות בדרגה 3 ומעלה זוהו בשלושה מטופלים; עם זאת, כל הרעילויות החמורות היו קשורות להתקדמות המחלה ולא לטיפול. לא נצפה הבדל משמעותי באיכות החיים הקשורה לבריאות (HRQoL) בזמן ההערכה בעבור מטופלים שהיו זמינים לשאלונים.
מסקנה – טיפול קרינתי לכל הכבד (WLI) בשילוב עם היפרתרמיה נסבלו היטב, ללא רעילות חמורה הקשורה לטיפול, עם תגובה מבטיחה מגרורות מרובות בכבד, שמקורן מסרטן המעי הגס אשר עמידות לכימותרפיה.
מבוא
הכבד הוא האתר השכיח ביותר להתפזרות גרורתית של גידולים ממאירים במערכת העיכול, הקשורה לאספקת הדם ממחזור הדם הפורטלי (portal circulation). כ-25% מהחולים עם סרטן המעי הגס מאובחנים בתחילה עם גרורות בכבד ומחלה גרורתית מטכרונית בכבד (metachronous liver metastasis) מתגלה במהלך המעקב בעוד 50% שתחילה אובחנו עם מחלה מקומית (localized disease). באוכלוסייה נבחרת של כ-20% עד 25% מהחולים ישנן התוויות לכריתה כירורגית; עם זאת, כשני שליש מהמטופלים שעברו ניתוח כריתה לריפוי (curatively resected) מציגים הישנות של הכבד תוך שנתיים.
מתן טיפול כימותרפיה בדרך עירוי באופן סיסטמי (Systemic) או באמצעות עירוי לעורק הכבד (hepatic arterial infusion) הוא הטיפול העיקרי בגרורות בכבד, אפילו בעבור מטופלים שעברו ניתוח כריתה לריפוי (curatively resected). עם הפיתוח והבחירה המתאימה של כימותרפיה, תוצאות ההישרדות (survival outcomes) משתפרות אצל מטופלים אלה. עם זאת, במסגרת הכימותרפיה האינטנסיבית הסטנדרטית הנוכחית, ההתקדמות התוך-כבדית (intrahepatic progression) ממשיכה בתוך 10 חודשים. למרות שניתן לשקול משטר נוסף של כימותרפיה בחולים נבחרים, הוא אינו מיועד עבור לתת-קבוצות של חולים בגלל תפקודי כבד, סטטוס התפקוד (performance status) או גורמים אחרים.
טיפול קרינתי לכל הכבד (WLI) הוא אפשרות פליאטיבית (palliative option) לגרורות נרחבות בכבד הגורמות לכאבים כתוצאה ממתיחה של קפסולת הכבד (liver capsule) ולהידרדרות בתפקודי הכבד. למרות שטיפול קרינתי לכל הכבד (WLI) מדגים יעילות מקובלת להקלה על הסימפטומים ב-55% עד 80% מהמטופלים, השליטה המקומית אינה משביעת רצון, בשל המגבלות של מינוני קרינה הניתנים למסירה הקשורים לרגישות האינטרינזית לטיפול בקרינה (intrinsic radiosensitivity) של הכבד. על מנת לשפר את התוצאות של טיפול קרינתי לכל הכבד (WLI), נבחנו במקביל רדיוסנסטיזטורים (radiosensitizers) או כימותרפיה. עם זאת, התוצאות מושפעות רק במידה מתונה עם העלייה המשמעותית ברעילות.
היפרתרמיה היא שיטת טיפול אדג'ובנטית ידועה לטיפול בהקרנות לסרטן השד, צוואר הרחם ולסרטן פי הטבעת. מבחינה תיאורטית, היפרתרמיה משפרת את ההרג של תאי הגידול הידועים כעמידים לקרינה (radioresistant). בנוסף, מספר ניסויים אקראיים מבוקרים הדגימו יתרונות לשליטה מקומית-אזורית (locoregional control) באמצעות קידום אפקט הרגישות לטיפול בקרינה (radiosensitizing effects). בהתבסס על רקע זה, החוקרים תכננו ניסוי פאזה 2, לצורך הערכת היעילות והרעילות של טיפול קרינתי לכל הכבד (WLI) בשילוב עם היפרתרמיה עבור חולים עם גרורות מרובות בכבד, שמקורן מסרטן המעי הגס אשר עמידות לכימותרפיה (chemorefractory).
חומרים ושיטות
ועדת הביקורת המוסדית אישרה מחקר זה (IRB No. 2013-06-040) וכל המטופלים נתנו הסכמה מדעת בכתב לפני הגיוס למחקר. ניסוי זה רשום בכתובת-clinicaltrials.gov (NCT01963117). רשימות הפרוטוקול והסטנדרטים המגובשים של דיווח ניסויים (Reporting Trials) (CONSORT) של הניסוי הנוכחי זמינים במידע התומך.
מטופלים
כל המטופלים היו צריכים להיות עם סרטן המעי הגס שאושר פתולוגית עם גרורות מרובות בכבד, אשר בלתי ניתנות לניתוח (unresectable) ועם עמידות לכימותרפיה. מטופלים גויסו למחקר הנוכחי על פי קריטריוני הכשירות הבאים: גיל 20 ומעלה; תפקוד תקין של מח העצם (המוגלובין מעל 8 גרם/ד"ל; ספירת נויטרופילים אבסולוטית מעל 1,500/μL; ספירת טסיות מעל 50,000/μL), תפקודי כבד תקינים (זמן פרותרומבין {prothrombin time}-ליחס בינלאומי מנורמל {international normalized ratio} פחות מ-1.7; אלבומין ≥ 2.8 גרם/ד"ל, אספרטאט {aspartate} או אלנין טראנסאמינאז {alanine aminotransferase} נמוך מפי 6). החוקרים לא כללו מטופלים שהיו להם פחות מ-8 שבועות של הישרדות צפויה (expected survival), שקיבלו בעבר טיפולי הקרנות בבטן העליונה או כאלה שסבלו ממיימת בלתי נשלטת (uncontrolled ascites), נשימה בלתי יציבה הקשורה לתפליט פלאורלי (pleural effusion), או מחלת ריאות חסימתית כרונית (chronic obstructive pulmonary disease). חולים עם סטטוס תפקודי (performance status) בדרגה 4 של קבוצת הקואופרטיב האונקולוגי המזרחי (Eastern Cooperative Oncology Group- ECOG)לא נכללו גם כן. כל האינדיקציות האפשריות למחקר נדונו לפני הרישום על ידי ועדת גידולי המעי הגס (colorectal tumor board) של מנתחים, גסטרואנטרולוגים, אונקולוגים רפואיים ואונקולוגים קרינתיים.
הפרוטוקול תוקן פעם אחת בינואר 2014 עקב צבירה איטית של חולים, מה שהרחיב את האינדיקציה מסרטן המעי הגס הראשוני לממאירות ראשונית של מערכת העיכול, אך בסופו של דבר גויסו רק ממאירויות של המעי הגס.
טיפולי הקרנות
על מנת להימנע מהחמצת מטרות הקשורות לתנועה נשימתית, נעשה שימוש בפרוטוקולי הנחיה של תמונה מלאה (full-image guidance) בכל המטופלים. אימון הנשימה נערך באמצעות הדרכה אודיו-ויזואלית לפני סימולציה כדי לשפר את מחזוריות הנשימה והדרכת נשימה אודיו-ויזואלית שימשה במהלך סימולציות ומתן טיפולי הקרנות. בסימולציות נעשה שימוש ב-GE LightSpeed בתוספת 16 סורקים (GE Healthcare, Milwaukee, WI, USA). חומר ניגוד תוך ורידי (Visipaque 270; Amersham Health Centre, Amersham, UK; 2 מ"ל/ק"ג עבור מקסימום 200 מ"ל) הוזרק בקצב של 5 מ"ל/שנייה. סריקות טומוגרפיה ממוחשבת (computed tomography) מסוג שלExhale breath-hold הושגו לאחר 50 עד 60 שניות. לאחר מכן, סריקות טומוגרפיה ממוחשבת ארבע-ממדיות נעשו שוב, באמצעות מערכת ניהול המיקום בזמן אמת (Real-time Position Management system) (Varian Medical Systems, Palo Alto, CA, USA).
נפח היעד הקליני (Clinical target volume) הוגדר ככל הכבד בהדמיות טומוגרפיה ממוחשבות. נפח היעד הפנימי (Internal target volume) הוגדר כסכום של נפח היעד הקליני (CTV) עבור כל שלבי הנשימה (respiration phases). נפח יעד התכנון (Planning target volume) הוגדר כנפח היעד הפנימי (ITV) בתוספת מרווח שולי הגדרה (setup margin) של 5 מ"מ. התכנון הקונפורמי המרבי (conformal planning) נעשה באמצעות 3-5 אלומות משיקות (coplanar) או אלומות לא משיקות (noncoplanar beams) באנרגיה של 4 או 10 MV קרני רנטגן בטכניקת שדה בשדה (field-in-field technique). מינוני הקרינה נקבעו ל-21 greys (Gy) ב-7 שברים תוך שימוש בפרוטוקול של הניסוי הקודם של קבוצת הקרינה האונקולוגית RTOG (Radiation Therapy Oncology Group).
היפרתרמיה
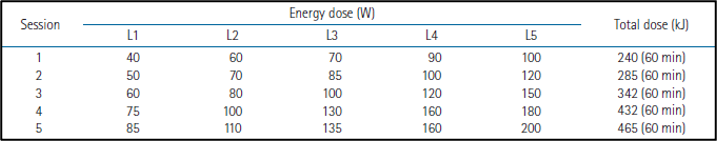
הטיפול בהיפרתרמיה התבצע באמצעות מערכת אלקטרו-היפרתרמיה (electrohyperthermia) של Celsius TCS (Celsius42+ GmbH, Cologne, Germany) למשך 60 דקות פעמיים בשבוע, במרווחים של 72 שעות לפחות, למשך 5 מפגשי טיפול בסך הכל ממועד הסימולציה. במפגש הטיפול השלישי, היפרתרמיה בוצעה מיד לאחר המקטע הראשון של הטיפול הקרינתי לכל הכבד (WLI); מפגשי הטיפול הרביעי והחמישי בוצעו גם כן לאחר הטיפול הקרינתי לכל הכבד (WLI) תוך שימוש בפרוטוקול של פעמיים בשבוע (twice-a-week protocol). ככל האפשר, הכבד כולו נכלל בתוך אזור ההיפרתרמיה בגדול של 20 × 20 סמ"ר. סכמת ההאצה האנרגטית (energy escalation) מוצגת בטבלה משלימה 1. במכשיר זה, על מנת להפחית את האפשרות של כוויות בעור, סופקה מערכת קירור שהופעלה במהלך פגישת הטיפול בהיפרתרמיה. טמפרטורת העור נוטרה באופן רציף באמצעות שלושה חיישני סיבים אופטיים מזכוכית (glass fiber-optic sensors) במהלך מפגשי הטיפולי בהיפרתרמיה.
להלן טבלה משלימה 1: סכמת ההאצה האנרגטית של היפרתרמיה במחקר של WHITHER
הערכת איכות חיים הקשורה לבריאות (HRQoL)
איכות חיים הקשורה לבריאות (HRQoL) הוערכה בנקודת ההתחלה ובחודש, חודשיים ו-3 חודשים לאחר הטיפול, באמצעות הגרסה הקוריאנית של שאלון איכות החיים של הארגון האירופי לחקר וטיפול בסרטן C-30 (EORTC QLQ-C30) וההערכה הפונקציונאלית של טיפול בסרטן–כבד ודרכי מרה גרסה 4.0 (FACT-Hepatobiliary v4.0). בזמן הערכת איכות החיים הקשורה לבריאות (HRQoL), סטטוס הכאב הנוכחי הוערך גם עם הסולם האנלוגי חזותי (VAS-visual analog scale) עבור כאב.
מעקב והערכת רעילות
הערכת המעקב הראשונה תוכננה להתקיים חודש אחד לאחר הטיפול הקרינתי לכל הכבד (WLI) עם טיפול בהיפרתרמיה, ולאחר מכן כל חודש למשך 3 חודשים. בכל הערכת מעקב, עברו המטופלים בדיקות קליניות ובדיקות גופניות. הוערכו איכות חיים הקשורה לבריאות (HRQoL), סולם אנלוגי חזותי (VAS) לכאב ואנטיגן קרצינואמבריוני (Carcinoembryonic Antigen – CEA). בוצעה סריקת טומוגרפיה ממוחשבת (CT), ונבדק פרופיל כימיה (chemistry profiling) כולל תפקודי כבד.
רמות הרעילות הוערכו באמצעות הקריטריונים הטרמינולוגיים המשותפים לתופעות לוואי גרסה 4.0 (Common Terminology Criteria for Adverse Events).
ניתוח סטטיסטי
ניסוי זה תוכנן כמחקר פאזה שנייה. החוקרים תכננו לגייס 47 מטופלים על מנת לצפות בשיעור של 50% בפליאציה של הסימפטומים (symptom palliation rate), שהוגדרה כתגובת כאב מלאה (pain response) או חלקית במעקב של חודש אחד לאחר הטיפול הקרינתי לכל הכבד (WLI) עם היפרתרמיה. המחקר נאמד כבעל עוצמה סטטיסטית (power to detect) של 80% לזהות הבדל של 20% מטיפול קרינתי לכל הכבד (WLI) בלבד ברמת מובהקות דו-צדדית של 5%. תגובת הכאב, כנקודת הקצה העיקרית, הוערכה במעקב של חודש אחד עם קריטריונים של קבוצת הקונצנזוס הבינלאומי לגרורות בעצמות IBMCG (Bone Metastases Consensus) (טבלה משלימה 2).
להלן טבלה משלימה 2: The International Bone Metastases Consensus Group criteria

תגובות אובייקטיביות הוערכו במעקב של חודש אחד לפי הקריטריונים המעודכנים להערכת תגובה בגידולים מוצקים (Response Evaluation Criteria in Solid Tumors v1.1). מדידות חוזרות של ניתוח שונות חד כיווני (ANOVA-Analysis of variance) שימוש על מנת לקבוע שינויים באיכות החיים הקשורה לבריאות (HRQoL). התפלגויות של משתני זמן עד למאורע (time-to-event) נאמדו באמצעות שיטת קפלן-מאייר (Kaplan-Meier product-limit method) והושוו באמצעות מבחן לוג הדרגות (log-rank test). הישרדות ללא התקדמות מקומית (Local progression-free survival), המוגדרת כהתקדמות בתוך הכבד על פי RECIST v1.1 והישרדות ללא התקדמות הכאב (pain progression-free survival), המוגדרת כהתקדמות על פי הקריטריונים של IBMCG, חושבו מתאריך התחלת הטיפול הקרינתי לכל הכבד (WLI) ועד למועד התפתחות האירוע (event developed) או ביקור המעקב האחרון.
תוצאות
מטופלים
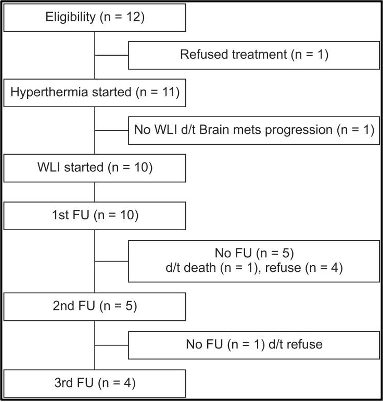
המחקר הסתיים מוקדם מכיוון שהצבירה הייתה נמוכה מהצפוי: 12 מטופלים הסכימו ונרשמו מנובמבר 2013 עד אוגוסט 2014. אחד סירב להמשך טיפול לפני הסימולציה ואחר לא קיבל הקרנה לאחר סימולציה בגלל התקדמות של גרורות במוח. מעקב היה זמין עבור 10 מטופלים לאחר חודש אחד, עבור חמישה מטופלים לאחר חודשיים, וארבעה מטופלים לאחר 3 חודשים בעקבות טיפול קרינתי לכל הכבד (WLI) עם היפרתרמיה (איור 1), וב-10 המטופלים שקיבלו טיפול קרינתי לכל הכבד (WLI) בוצעה אנליזה.
להלן איור 1: דיאגרמת סטנדרטים מאוחדים של ניסויים בדיווח (CONSORT)
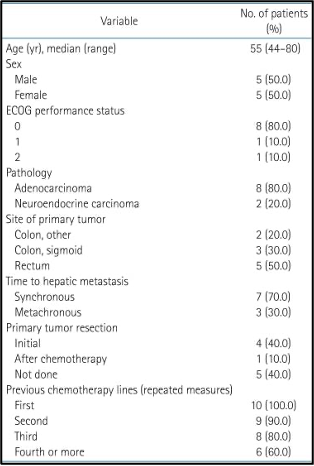
המאפיינים הדמוגרפיים והבסיסיים של 10 המטופלים שנרשמו לקבלת טיפול מוצגים בטבלה 1. הגיל החציוני היה 55 שנים (טווח של 44 עד 80 שנים). למטופל אחד היה סטטוס תפקודי של ECOG 2. קרצינומה נוירואנדוקרינית (Neuroendocrine carcinoma) נמצאה אצל 20%. לכל המטופלים שנרשמו הייתה היסטוריה של התקדמות לאחר לפחות משטר טיפול אחד של כימותרפיה.
להלן טבלה 1: מאפייני המטופלים
הטיפול הקודם
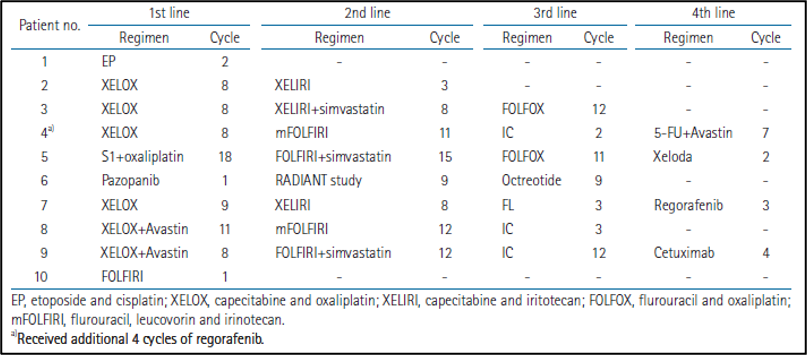
המספר החציוני של מחזורי כימותרפיה שניתנו לפני הרישום למחקר היה 23 (טווח של 1 עד 46).נעשה שימוש ביותר מ-10 מחזורים של כימותרפיה, למעט בשני מטופלים עם התקדמות נרחבת של גרורות בכבד לאחר התחלת משטר הכימותרפיה הראשון. מטופלים אלו לא יכלו לקבל כימותרפיה נוספת בשל החמרה בתפקודי הכבד. משטרי טיפול הכימותרפיה הנפוצים היו קפציטבין (capecitabine) ואוקסליפלטין (oxaliplatin) או פלואורואורציל (5-fluorouracil), עם לויקובורין (leucovorin) ואירינוטקאן (irinotecan) עבור אדנוקרצינומה (adenocarcinoma) או אטופוסיד (etoposide) עם ציספלטין (cisplatin) או אוקטריאוטיד (octreotide) עבור קרצינומה נוירואנדוקרינית (neuroendocrine carcinoma). משטרי כימותרפיה מפורטים מוצגים בטבלה משלימה 3. רדיותרפיה פליאטיבית (Palliative RT) ניתנה לשני מטופלים עם מסות ראשוניות (primary masses) ולמטופל אחד עם גרורות בעמוד השדרה (spine metastasis) עם דחיסה של חוט השדרה (spinal cord compression).
להלן טבלה משלימה 3: משטרי כימותרפיה מפורטים של המטופלים הרשומים
קרינה של כל הכבד (Whole hepatic irradiation) בשילוב עם היפרתרמיה
למעט המטופל שסירב להמשך טיפול לאחר 6 מקטעים של טיפול קרינתי לכל הכבד (WLI), כל המטופלים השלימו את המינון הכולל המתוכנן של 21 Gy. חמישה מפגשי טיפול ההיפרתרמיה המתוכננים הושלמו בשמונה מטופלים, אם כי היה צורך בהפחתת אנרגיה של כ-10% בשניים מהם בגלל כאב הקשור להיפרתרמיה. שני מטופלים נוספים סירבו להיפרתרמיה נוספת לאחר פגישת הטיפול השלישית והרביעית בגלל כאבים. במהלך ההיפרתרמיה, הטמפרטורות של פני העור נשמרו על בין 36 מעלות צלזיוס עד ל-37.5 מעלות צלזיוס בכל המטופלים.
תגובת כאב
מתוך 10 מטופלים שקיבלו טיפול קרינתי לכל הכבד (WLI) עם היפרתרמיה, לאחר חודש אחד, נצפתה תגובה חלקית (partial response) בארבעה מטופלים עם מחלה יציבה (stable disease). לאחר חודשיים, מטופל אחד עם תגובה חלקית (PR) הומר לתגובה מלאה (complete response), שני מטופלים הציגו מחלה פרוגרסיבית (progressive disease), ומטופל אחד הדגים מחלה יציבה (SD). לא נצפה שינוי בכאב לאחר 3 חודשים. הציון החציוני של הסולם האנלוגי החזותי (VAS) היה 4.0 (טווח בין 0 עד 10), 3.5 (טווח בין 0 עד 7), 3.0 (טווח בין 0 עד 7) ו-0 (טווח בין 0 עד 9) לפני ובחודש, חודשיים ו-3 חודשים לאחר טיפול בקרינה, בהתאמה.
תגובה אובייקטיבית (Objective response) של גרורות בכבד
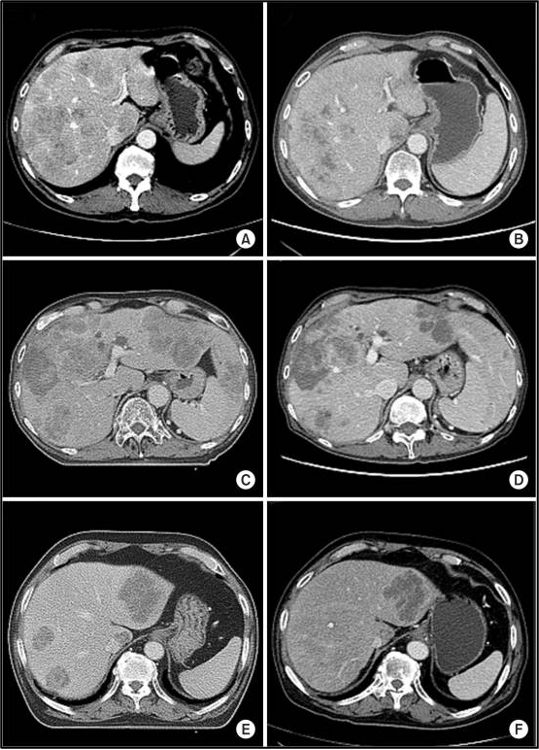
מתוך 10 המטופלים שקיבלו טיפול קרינתי לכל הכבד (WLI) עם היפרתרמיה, מחלה פרוגרסיבית (PD) של גרורות בכבד נצפתה בשני מטופלים (20%), ושלושה הציגו תגובה חלקית (PR) (איור 2). לאחר חודשיים, השלושה האחרים הציגו מחלה פרוגרסיבית (PD) בכבד, ושלושה נותרו ללא מחלה פרוגרסיבית (PD-free) 3 חודשים לאחר הטיפול.
להלן איור 2 : שינויים בתמונות ההדמיה של טומוגרפיה ממוחשבת (CT) לאחר טיפול קרינתי לכל הכבד (WLI) בשילוב עם היפרתרמיה: 3 מתוך 10 מטופלים הדגימו תגובה חלקית (partial response) חודש אחד אחרי הטיפול. תמונות הדמיית CT שנלקחו לפני (A,C,E) וחודש אחרי WLI (F,D,B)
שינוי מעבדתי ותופעות לוואי לאחר טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה
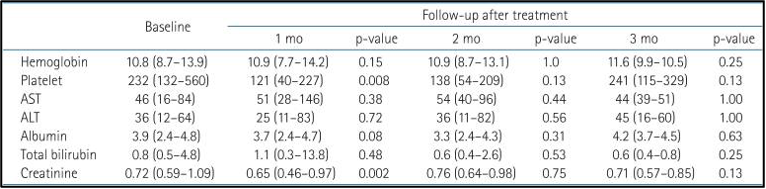
במהלך תקופת הטיפול והמעקב התגלו רעילות בדרגה 3 ומעלה בארבעה מטופלים. שינוי מעבדתי מקו הבסיס בחודש, חודשיים ו-3 חודשים לאחר היפרתרמיה וטיפול קרינתי לכל הכבד (WLI) מוצג בטבלה 2.
להלן טבלה 2: שינוי מעבדתי לאחר טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה
איכות חיים הקשורה לבריאות (HRQoL)
הערכת איכות חיים הקשורה לבריאות (HRQoL) הייתה אפשרית רק בחלק קטן מהמטופלים שנרשמו עקב אובדן למעקב (loss to follow-up). איכות חיים הקשורה לבריאות (HRQoL) הוערכה בתחילת המחקר בכל המטופלים, לאחר חודש בחמישה מטופלים, לאחר חודשיים בארבעה מטופלים ובשלושה חודשים בארבעה מטופלים.
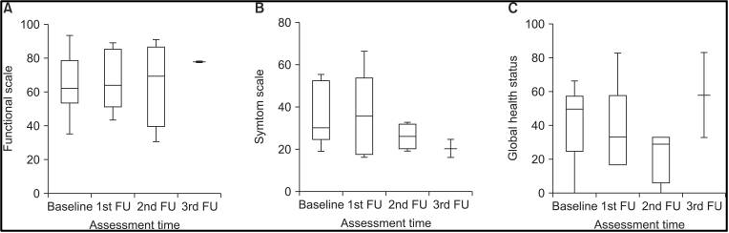
לא נמצאו הבדלים מובהקים באיכות החיים הקשורה לבריאות (HRQoL) בזמן ההערכה במטופלים שיכלו לענות על השאלון, הן EORTC QLQ-C30 (איור 3) והן FACT-Hep (איור 4). ציוני איכות החיים הקשורים לבריאות (HRQoL) נטו בדרך כלל להשתפר עם המעקב. עם זאת, סטטוס הבריאות הגלובלי (global health status) וסולמות הסימפטומים (symptom scales) של EORTC QLQ-C30 ירדו מעט במהלך המעקב.
להלן איור 3: שינוים ב-EORTC QLQ-C30, תתי סולמות מקו הבסיס ל3 חודשים לאחר טיפול קרינתי לכל הכבד בשילוב עם היפרתרמיה. (A) סולם תפקודי, (B) סולם סימפטומים, (C) סטטוס בריאות גלובלי.
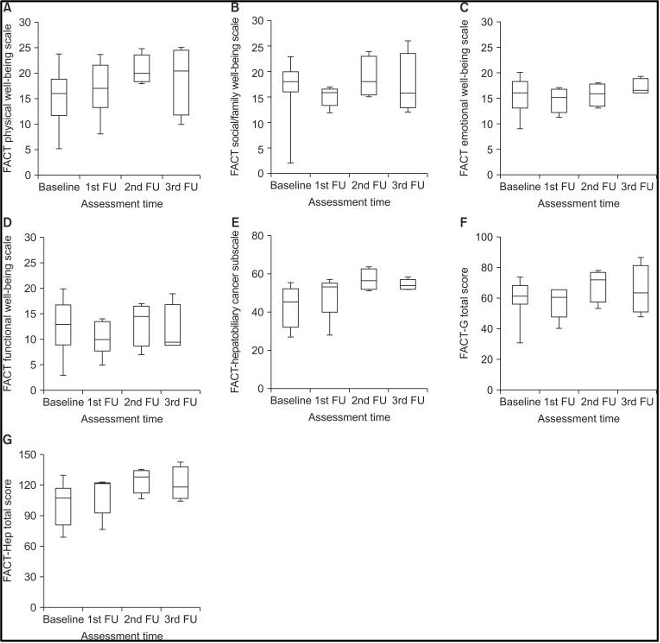
להלן איור 4: שינויים ב-FACT-Hep, תתי סולמות מקו הבסיס ל3 חודשים לאחר טיפול קרינתי לכל הכבד בשילוב עם היפרתרמיה. (A) רווחה גופנית, (B) רווחה חברתית ומשפחתית, (C) רווחה רגשית, (D) רווחה תפקודית, (E) hepatobiliary cancer subscale, (F) FACTGeneral, (G) FACT-Hep total scores
הישרדות ללא התקדמות מקומית (local progression-free survival) והישרדות ללא התקדמות כאב (pain progression-free survival) -
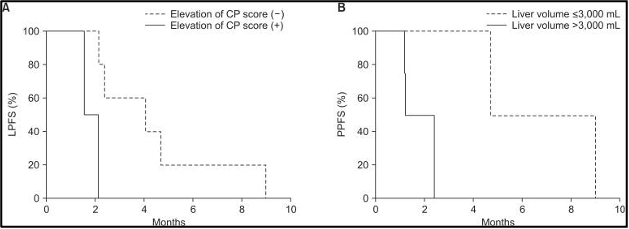
לאחר 3 חודשים, ההישרדות ללא התקדמות מקומית (LPFS) הייתה 30% וההישרדות ללא התקדמות כאב (PPFS) הייתה 58.3%. גורמים פרוגנוסטיים אפשריים הקשורים לשיעורי ההישרדות נמצאים בטבלה 3. עלייה בדירוג צ'יילד-פו (Child-Pugh score) (p = 0.04) (איור 5A) בחודש אחד לאחר טיפול קרינתי לכל הכבד (WLI) עם היפרתרמיה היה גורם פרוגנוסטי משמעותי להישרדות ללא התקדמות מקומית (LPFS). הישרדות ללא התקדמות מקומית (LPFS) נוטה להיות גבוהה יותר במטופלים ללא גרורות חוץ-כבדיות משולבות (combined extrahepatic metastasis) (p = 0.1) (איור משלים 1).
לא נמצאו הבדלים מובהקים באיכות החיים הקשורה לבריאות (HRQoL) בזמן ההערכה במטופלים שיכלו לענות על השאלון, הן EORTC QLQ-C30 (איור 3) והן FACT-Hep (איור 4). ציוני איכות החיים הקשורים לבריאות (HRQoL) נטו בדרך כלל להשתפר עם המעקב. עם זאת, סטטוס הבריאות הגלובלי (global health status) וסולמות הסימפטומים (symptom scales) של EORTC QLQ-C30 ירדו מעט במהלך המעקב.
להלן איור 5: עקומות ההישרדות של קפלן-מאיר בהתאם לגורמים פרוגנוסטיים מובהקים. (A) עלייה בדירוג צ'יילד-פו (CP) בחודש אחד על ההישרדות ללא התקדמות מקומית (LPFS), (B) נפח כבד שלם (Whole liver volume) גדול מ-3,000 מ"ל המייצג נפח גידול גרורתי על ההישרדות ללא התקדמות כאב (PPFS)
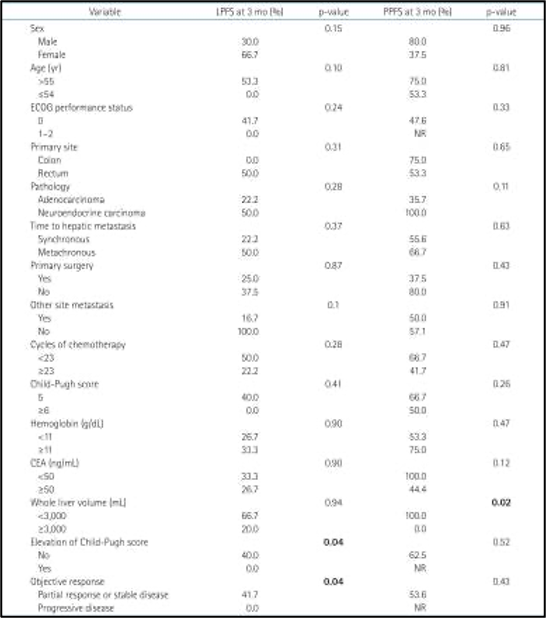
להלן טבלה 3: גורמים פרוגנוסטיים אפשריים בעבור הישרדות ללא התקדמות מקומית (LPFS) וההישרדות ללא התקדמות כאב (PPFS)
נפח כבד שלם (Whole liver volume) גדול מ-3,000 מ"ל (p = 0.02) (איור 5B), אשר ייצג בעקיפין נפח גידול גרורתי (metastatic tumor volume), היה קשור באופן מובהק להישרדות ללא התקדמות כאב (PPFS) נמוכה יותר. הישרדות ללא התקדמות כאב (PPFS) נוטה להיות גבוהה יותר במטופלים עם קרצינומה נוירואנדוקרינית (neuroendocrine carcinoma) (p = 0.11) (איור משלים 2) ורמה ראשונית של אנטיגן קרצינואמבריוני (CEA) גבוהה מ-50 ננוגרם/מ"ל (p = 0.12) (איור משלים 3). תגובה אובייקטיבית (Objective response) לאחר חודש אחד לא הייתה קשורה להישרדות ללא התקדמות כאב (PPFS) (p =0.43).
איור משלים 1: עקומת ההישרדות של קפלן-מאיר של ההישרדות ללא התקדמות מקומית (LPFS) בהתאם לנוכחות של גרורות חוץ כבדיות משולבות
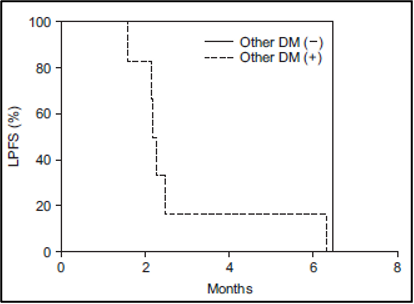
איור משלים 2: עקומת ההישרדות של קפלן-מאיר של ההישרדות ללא התקדמות כאב (PPFS) בהתאם לפתולוגיה של הגידול הראשוני
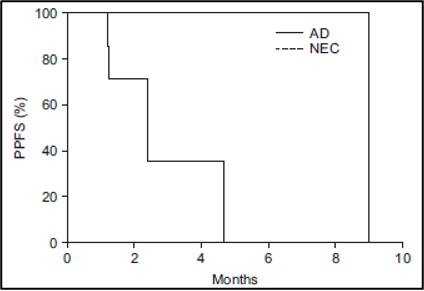
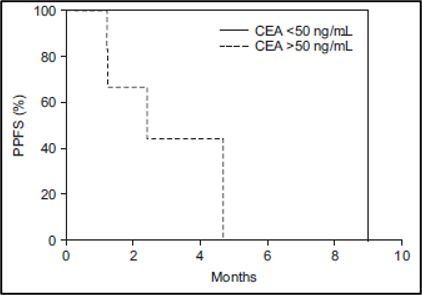
איור משלים 3: עקומת ההישרדות של קפלן-מאיר של ההישרדות ללא התקדמות כאב (PPFS) בהתאם לרמה הראשונית של האנטיגן הקרצינואמבריוני (CEA)
דיון ומסקנות
הכבד הוא איבר הרגיש לקרינה (radiosensitive). רעילות כבד הנגרמת על ידי קרינה היא עדיין בעיה לא פתורה בטיפול בהקרנות מכוונות כבד (liver-directed RT). הידרדרות בתפקוד הכבד לאחר טיפול פליאטיבי קרינתי לכל הכבד (WLI) במטופלים עם גרורות בלתי נשלטות בכבד העמידות לכימותרפיה נותרה דאגה של אונקולוגים קרינתיים.
מחקרים אחרונים הראו כי השכיחות הולכת ופוחתת, אך רעילות כבדית הנגרמת על ידי קרינה (radiation-induced hepatic toxicity) מתפתחת בתת-קבוצה קטנה של מטופלים המקבלים טיפולי הקרנות בעבור סרטן כבד ראשוני גם לאחר טיפולי קרינתי במינון נמוך. עם זאת, התנאים של כבד תקין, סרטן כבד גרורתי וסרטן כבד ראשוני הם שונים בבירור, מכיוון שמרבית סוגי סרטן הכבד הראשוניים מתפתחים ממחלות כבד כרוניות כגון שחמת הכבד (cirrhosis) או דלקת כבד נגיפית (viral hepatitis). מכיוון שהידרדרות בתפקוד הכבד בגרורות בכבד נובעת מעומס הגידולים הגרורתיים (metastatic tumor burden), תפקוד הכבד משתפר לאחר טיפול קרינתי לכל הכבד (WLI) במקום להיפגע. מחקר פרוספקטיבי של RTOG לא הדגים רעילות כבדית הנגרמת על ידי קרינה ב-109 מטופלים עם גרורות בכבד לאחר טיפול קרינתי לכל הכבד (WLI) במינון נמוך, כגון 21 Gy ב-7 מקטעים.
טיפול קרינתי לכל הכבד (WLI) במינון נמוך, היא גם שיטה פליאטיבית יעילה לכאבי בטן, בחילות או הקאות ומצבים אחרים. על פי הספרות, לפיכך, יש לשקול טיפול קרינתי לכל הכבד (WLI) במינון נמוך על מנת לשמור על איכות החיים הקשורה לבריאות (HRQoL) במטופלים עם גרורות כבד סימפטומטיות (symptomatic liver metastasis). למעשה, קבוצת הקונצנזוס לגרורות בכבד (Liver Metastases Consensus Group) מציעה כי טיפול קרינתי לכל הכבד (WLI) הוא בטוח ויעיל בעבור גרורות כבד סימפטומטיות, בהתבסס על סקירה של נתונים קליניים זמינים.
הקבוצה של החוקרים במחקר הנוכחי, דיווחה בעבר על תוצאות של מחקר רטרוספקטיבי של טיפול קרינתי לכל הכבד (WLI) כ-21 Gy ב-7 מקטעים, ב-16 מטופלים עם גרורות בכבד של סרטן המעי הגס. פליאציה של כאבי בטן הייתה מקובלת, אך חציון ההישרדות הכוללת (overall survival) היה 9 שבועות בלבד. הערכת התגובה האובייקטיבית (Objective response) לא הייתה אפשרית בגלל מעקב קצר. על פי מחקרים אחרים המשתמשים באותו מינון טיפול קרינתי לכל הכבד (WLI), תגובה מינימלית בלבד מושגת בחלק קטן מהמטופלים. למרות של טיפול קרינתי לכל הכבד (WLI) במינון נמוך הוא שיטה פליאטיבית יעילה, יש צורך בשיטה שיכולה לשפר את התגובה המקומית ולשמור על ההשפעות של טיפול הקרינה בכבד התקין. לפיכך, החוקרים ערכו ניסוי פרוספקטיבי בפאזה שנייה, על מנת להעריך את התגובה ותופעות הלוואי משילוב של טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה עבור גרורות בכבד שמקורן מסרטן המעי הגס אשר עמידות לכימותרפיה.
בקרב מומחים לאונקולוגיה קרינתית, היפרתרמיה היא רדיוסנסיטייזר מוכר היטב. היפרתרמיה יעילה בשלב ה-S, ב-pO2 נמוך, pH נמוך ואזורים עם פרפוזיה נמוכה הידועים כעמידים לקרינה (radiosensitizer).שיפור בשליטה המקומית-אזורית (locoregional control) באמצעות טיפולי הקרנות משולבים עם היפרתרמיה דווחו במספר אתרי סרטן, כגון השד, צוואר הרחם והראש והצוואר.
בדומה לתוצאות של מחקרים פרוספקטיביים ורטרוספקטיביים אחרים של טיפול קרינתי לכל הכבד (WLI) במינון נמוך, בקרב רוב המטופלים בניסוי הנוכחי של החוקרים, הטיפולים משולבים של טיפול קרינתי לכל הכבד במינון נמוך (WLI) והיפרתרמיה היו נסבלים. תופעות לוואי בדרגה 3 ומעלה התפתחו בגלל התקדמות של מחלה מרוחקת או תוך-כבדית. למרות שכמעט מחצית מהמטופלים לא עברו מעקב כמתוכנן, החוקרים לא היו מודעים לרעילות כבדית הנגרמת על ידי קרינה.
תגובה אובייקטיבית חלקית (Partial objective response) הושגה אצל שלושה מטופלים לאחר טיפול משולב. בהתחשב בכך שרוב המטופלים שנרשמו קיבלו יותר מ-10 מחזורים של כימותרפיה, אשר עשוי להיות גורם ניבוי שלילי (negative predictive factor) לתגובת הקרינה, שיעור התגובה לא היה מאכזב. עם זאת, הישרדות ללא התקדמות מקומית (LPFS) עדיין הייתה בלתי מקובלת בחציון של 2.2 חודשים. לכן, טיפול סיסטמי נוסף במטופלים המציגים תגובה חיובית לאחר הטיפול והתאוששות של תפקודי הכבד יכול להיות אפשרות. ההישרדות ללא התקדמות מקומית (LPFS) הייתה מעט נמוכה יותר במטופלים עם גרורות משולבות (combined metastasis) לאתרים אחרים מלבד הכבד, כך שיישום מוקדם יותר של טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה עשויה להיות אפשרות נוספת.
למרות שאיכות חיים הקשורה לבריאות (HRQoL) הוערכה בפחות ממחצית מהמטופלים 2-3 חודשים לאחר הטיפול, איכות החיים הקשורה לבריאות (HRQoL) נשמרה במטופלים שהוערכו. בדומה לאיכות חיים הקשורה לבריאות (HRQoL), התקדמות הכאב בהתאם לקריטריונים של IBMCG התעכבה עד לחציון של 4.7 חודשים. בנוסף, התקדמות הסימפטומים הייתה קשורה בבירור לנפח הכבד כולו (whole liver volume) המייצג את עומס הגידולי הגרורתי (metastatic tumor burden). לא נצפתה התקדמות כאב במטופלים עם נפח הכבד כולו (whole liver volume) של פחות מ-3,000 מ"ל במהלך המעקב.
לכן, יישום מוקדם יותר של טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה עשוי להיות אפשרות תקפה להשגת שליטה מקומית מקסימלית (maximum local control) ללא התקדמות כאב עבור מטופלים עם גרורות כבד העמידות בפני כימותרפיה עם עומס גרורתי (metastatic burden) קטן יותר וגרורות מוגבלות בלבד (metastasis confined). אבל יש לקחת בחשבון שמחקר זה אינו קובע באופן סופי את היעילות האמיתית של שילוב בין טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה בגלל גודל המדגם הקטן, תכנון הזרוע הבודד וסגירה מוקדמת של המחקר.
למחקר זה היו כמה מגבלות. ראשית, הוא הסתיים מוקדם בגלל צבירה לקויה של מטופלים ושיעור גבוה של אובדן למעקב (follow-up loss). רק 40% מהמטופלים היו במעקב כמתוכנן בעיקר בשל סירוב המטופלים. תופעה זו עשויה להיות תוצאה של הקריטריונים לזכאות למחקר הנוכחי, שכללו מטופלים שלא תכננו טיפול נוסף או שרצו טיפול תומך בלבד. לכן, התוצאות של המחקר הנוכחי אינן מספיקות כדי להעריך את היעילות והבטיחות האמיתיות בגלל האוכלוסייה המצומצמת והכמות המוגבלת של נתוני הערכה. בנוסף, היפרתרמיה עשויה להינתן באופן לא אופטימלי במטופלים עם נפח גידול גדול יותר בשל מגבלה של אפליקטור. יותר מכל, הניתוח של הגורמים הפרוגנוסטיים עשוי להיות מוגבל בשל גודל המדגם הקטן. שנית, החוקרים לא יכלו להעריך את הטמפרטורה האמיתית של אזור הגידול בגלל הפולשנות והנטייה לדימומים במטופלים שנרשמו.
לסיכום, שילוב בין טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה במטופלים עם גרורות מרובות בכבד, שמקורן מסרטן המעי הגס אשר עמידות לכימותרפיה עשוי להיות מבטיח ללא רעילות חמורה הקשורה לטיפול, אם כי החוקרים לא קבעו באופן חד משמעי, את היעילות האמיתית של השילוב בין טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה על פני טיפול קרינתי לכל הכבד (WLI) בלבד במחקר הנוכחי בגלל תכנון המחקר של הזרוע הבודדת. עם זאת, הסגירה המוקדמת של מחקר זה ואובדן רוב המטופלים למעקב הגבילו את יכולת החוקרים להעריך את יעילות הטיפול האמיתית. יש צורך במחקרים פרוספקטיביים מתוכננים היטב בקנה מידה גדול יותר, על מנת להעריך את היעילות והרעילות של טיפול קרינתי לכל הכבד (WLI) והיפרתרמיה עבור מטופלים עם גרורות מרובות בכבד, שמקורן מסרטן המעי הגס אשר עמידות לכימותרפיה.



