Retrospective Clinical Study of Advanced Pancreatic Cancer Treated with Chemotherapy and Abdominal Hyperthermia JGO – Journal of Global Oncology (4,1-4) by American Society of Clinical Oncology
Yu-Fei Fan, Beijing Yanhua Hospital; Yuan Qin and Ding-Gang Li, Beijing Haidian Hospital, Beijing, China; and David Kerr, University of Oxford, Oxford, United Kingdom
תקציר
מטרת המאמר – היפרתרמיה בשילוב עם כימותרפיה מהווה שיתוף מתקבל על הדעת כחלק מתיאור המנגנון, אם כי מנגנונים מולקולריים רבים המהווים את הבסיס לטיפול המשולב הזה עדיין אינם מובנים במלואם. מחקרים פרה-קליניים מצביעים על כך שקיימת סינרגיה פוטנציאלית עם גמציטבין (gemcitabine). מידע זה מספק את הבסיס לביצוע אנליזה רטרוספקטיבית של סדרת מקרים קלינים המשלבת סוג זה של טיפול בחולים עם סרטן לבלב מתקדם
חולים ושיטות – 29 מטופלים נאיביים לכימותרפיה, עם קרצינומה של הלבלב במצב מתקדם מקומית, או גידול גרורתי ושסבלו ממיימת עקב הממאירות – טופלו בציספלטין (Cisplatin) במתן תוך-צפקי (intraperitoneal) במינון של 30 מ"גm2 ובגמציטבין (gemcitabine) במינון של 800-1000 מ"גm2 במתן תוך ורידי ביום הראשון, השמיני וה15 כל 28 יום עד להתקדמות הטיפול. בנוסף המטופלים עברו טיפולי היפרתרמיה אזורית (regional) בין 41-42 מעלות צלזיוס באזור רום הבטן פעמיים בשבוע החל מהיום הראשון עד היום ה-21.
תוצאות – בסך הכל ניתנו כ-83 מחזורי כימותרפיה שנסבלו יחסית היטב. לא היו חולים שהראו תגובה מלאה, ל-13 הייתה תגובה חלקית, ל-7 מהם הייתה מחלה יציבה ול-9 הייתה מחלה מתקדמת. הישרדות ממוצעת של החולים ללא התקדמות ממוצעת והישרדות כוללת היו: 61±119 ימים ו-195 98± ימים, בהתאמה.
מסקנה – מחקר זה מספק ראיות ראשוניות על כך שגישת טיפול המשלבת כימותרפיה תוך-ורידית ותוך-צפקית יחד עם היפרתרמיה נסבלת היטב, פעילה ובעלת פרופיל הישרדות מתקבל על הדעת עבור חולים בסרטן הלבלב שלב 4 ומיימת.
מבוא
הנטל של סרטן הלבלב על מערכת הבריאות בסין הולך וגדל, עם שיעורי תמותה שנתיים שכמעט שווים לשיעורי ההיארעות, נעשה חישוב שהדגים כי בסין ישנם כמעט כ-20% מכלל המקרים החדשים בעולם.
בתת-הקבוצה של חולים עם סרטן לבלב מתקדם המתייצגים עם מיימת ממאירה, ההישרדות החציונית המדווחת היא נמוכה ביותר (63 -81 יום). הדרישה לפיתוח גישות טיפוליות חדשניות עבור קבוצה ספציפית זו בעל הפרוגנוזה הגרועה הוא ברור.
היפרתרמיה משתמשת בגלים אלקטרומגנטיים בתדר-גבוה בכדי לחמם תאים סרטניים ל45-41 °C. טמפרטורות מוגברות אלה יכולות לשנות את פתופיזיולוגית הסרטן ולהוביל לעליה בחדירות תאי הגידול והקלה במעבר דיפוזי של תרופות ציטוטוקסיות, מה שמצמצם והופך את העמידות הרב-תרופתית בתאי הגידול, מעכב את מנגנון התיקון של נזק לדנ"א, מעלה את ביטוי חלבוני ה-heat shock, הגברת האנטיגניות של הגידול ושיפור פעילות תאי NK (natural killer).
ישנן עדויות המראות שמתן תוך-צפקי של תרופות ציטוטוקסיות יוצר יתרון פרמקוקינטי, על ידי העברת ריכוז תרופות תוך-צפקי גבוה בהרבה בהשוואה למתן סיסטמי. הגברת החשיפה לתרופות ציטוטוקסיות של האזור המכיל את מרבית נטל הגידול עשויה להגדיל את שיעורי התגובה של הגידול. נושא זה הוכח בניסוי מבוקר גדול שהראה כי הזלפת ציספלטין במתן תוך-צפקי מעניק יתרון הישרדותי לחולים בסרטן השחלות בהשוואה למתן התוך-וורידי המקובל.
כאן, החוקרים מדווחים על הניסוי שביצעו בשימוש בכימותרפיה (גמציטבין תוך-ורידי יחד עם ציספלטין תוך-צפקי) בשילוב עם היפרתרמיה אזורית בגלי-רדיו כטיפול קו ראשון למטופלים עם סרטן לבלב מתקדם ומיימת.
חולים ושיטות
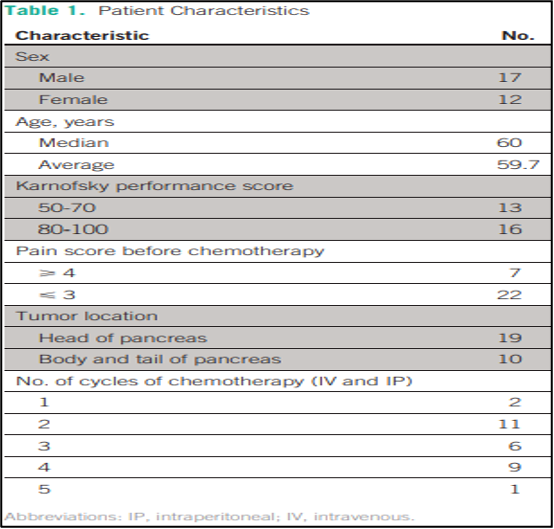
התוצאות התקבלו ממחקר רטרוספקטיבי של סדרת מקרים קלינים מכוונים פרוטוקול של חולים עוקבים שהגיעו לבית החולים יואנהואה בבייג'ין, סין. כל החולים חתמו על הסכמה מדעת למשטר הטיפול. למרות זאת, מכיוון שלא היה זה מחקר פרוספקטיבי קליני, לא נדרש אישור של ועדת הביקורת המוסדית. הגיוס התקיים בין השנים 2007-2012. מאפייני המטופל מסוכמים בטבלה 1.
להלן טבלה 1:
הליך הטיפול
לאחר ניקוז מיימת, צנתר תוך-צפקי (indwelling peritoneal catheter) הוכנס לתוך חלל הצפק תחת הרדמה מקומית. הצנתר אפשר מתן עירוי תוך-צפקי של ציספלטין במינון 30 מ"גm2 (ב2-2.5 ליטר של NACL למשך 30 דקות) ביום הראשון, השמיני וה-15. גמציטבין ניתן במינון 800-1000 מ"גm2 במתן תוך-ורידי בעירוי של 30 דקות ביום הראשון, השמיני וה-15 כל 28 יום עד שתועדה התקדמות בטיפול. בנוסף, המטופלים עברו טיפולי היפרתרמיה אזורית (regional) בין 41-42 מעלות צלזיוס למשך שעה באזור רום הבטן פעמיים בשבוע במשך שלושה שבועות (ביום הראשון, הרביעי השמיני ה-11, ה-15 וה-18) {מסוכם בטבלה 2}
המכשיר שהשתמשו בו היה מערכת היפרתרמיה " SR 1000 tumor hyperthermia system" מ- Beijing Xinke Establish Science and Technology. טמפרטורת היעד של האזור המטופל נקבעה על 42 מעלות צלזיוס. חום ניתן באמצעות זוג אלקטרודות שהונחו על הצדדים מנוגדים של אזור הכבד. כל אלקטרודה הייתה מכוסה ברפידת מים, ותמיסת סליין הנשמרה ב-5 מעלות הוזלפה לתוך הרפידות על מנת למנוע חימום יתר של העור והשומן התת-עורי. משך הטיפול בכל מפגש נע בין 40 עד 60 דקות (תלוי בסובלנות המטופל) בעוצמה של 150 וואט. מדדי לחץ הדם ודופק היו נוטרו כל 15 דקות במהלך ההיפרתרמיה. טמפרטורת הגוף נמדדה לפני ואחרי הטיפול.
להלן טבלה 2:

מדדי תוצא עיקריים
החולים הוערכו כדי להעריך את התגובה לטיפול (קריטריונים להערכת תגובה בגידולים מוצקים [RECIST]) ע"י טומוגרפיה ממוחשבת של הבטן (CT), דימות תהודה מגנטית (MRI) או בדיקת PET-CT. רעילות תועדה באמצעות שימוש בקריטריונים נפוצים של מינוח אירועים שליליים (CTCAE v3.0), הישרדות ללא-התקדמות המחלה (PFS) והישרדות כללי (OS) נמדדו החל מהיום הראשון של מחזור הטיפול הראשון. עקומות קפלן-מאייר בוצעו מנתוני הישרדות.
תוצאות
מאפייני המטופל
בסך הכל גויסו 29 חולים (17 גברים, 12 נשים); טווח הגילאים נע בין 34 ל-74 שנים, עם גיל חציוני של 60. הגידולים ראשוניים היו ממוקמים בעיקר בראש הלבלב והצוואר (n = 19), ושאר הגידולים היו ממוקמים בגוף הלבלב ובזנב (n=10). על פי הוועדה המשותפת האמריקאית לסרטן (AJCC; 7th Edition) לקביעת שלב המחלה, כל החולים היו בשלב 4 של המחלה. כל המטופלים היו נאיביים לכימותרפיה. טרום-כימותרפיה, סולם קרנופסקי (KPS) הציון של 13 חולים (44.8%) היה 50 עד 70, עבור 16 חולים (55.2%), זה היה 80 עד 100. כל ה-29 מטופלים השלימו סך של 83 מחזורי כימותרפיה (טווח, אחד עד חמישה מחזורים; חציון, שלושה מחזורים; טבלה 1)
ניתוח יעילות
מעקב באמצעות טכניקת ההדמיה המתאימה ביותר (CT, MRI, או PET-CT) בוצע כל שני מחזורי טיפול, וכל הסריקות נבדקו על ידי רדיולוג יחיד באמצעות קריטריונים RECIST. לא היו תגובות מלאות (CRs), ל-13 מטופלים (44.8%) היו תגובות חלקיות (PRs), ושבעה חולים (24.4%) היו עם מחלה יציבה(SD). תשעה חולים (31.0%) היו במחלה מתקדמת (PD). בסך הכל שיעור התגובה האובייקטיבי (CR + PR) היה 44.8%, ושיעור בקרת המחלות היה (CR + PR+ SD) 70.0%. ממוצע של PFS של כל הקבוצה (n = 29) היה 61±119 ימים וממוצע ה-OS היה 98±195 ימים.
ניתוח בטיחות
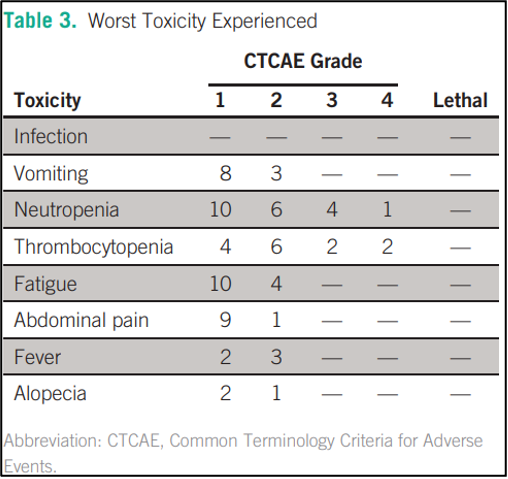
רעילות נפוצה כללה בחילה בדרגה 2 והקאות (10.3% מהחולים), טרומבוציטופניה בדרגה 3 או 4 (13.8%), עייפות בדרגה 2 או 3 (13.8%), נויטרופניה בדרגה 3 או 4 (17.2%). דרגה 1 או 2 של חום נמצאה ב-17.2% מהחולים ודרגה 1 או 2 של כאבי בטן נמצאו ב-34.5% לאחר ציספלטין (Cisplatin) במתן תוך-צפקי. כאבי הבטן השתפרו לאחר הגדלת נפח התמיסה הפיזיולוגית ששימשה לעירוי התוך-צפקי. {מסוכם בטבלה 3}
להלן טבלה 3:
דיון
מחקר רטרוספקטיבי קטן זה של סדרת מקרים קלינים מצביע על כך שגישת טיפול המשלבת הזלפת כימותרפיה תוך-ורידית של gemcitabine יחד עם cisplatin תוך-צפקית בשילוב עם היפרתרמיה נסבלה היטב בקרב חולים עם סרטן לבלב מתקדם ומיימת כתוצאה מהממאירות. גישה טיפולית זו הציעה קצב שליטה יוצא מן הכלל במחלה ובהתאם גם בשיעור ההישרדות הכללי (OS) במיוחד בקבוצתה חולים העמידים. הטיפול הסטנדרטי בסרטן הלבלב התפתח בעשור האחרון, מטיפול בתרופה אחת כמו גמציטבין, למשטרי טיפול מורכבים יותר כגון, fluorouracil, leucovorin, irinotecan ו oxaliplatin (FOLFIRINOX).
מחקר גדול שנערך הראה כי מטופלים במצב תפקודי טוב עם סרטן לבלב מתקדם שטופלו ב- FOLFIRINOX שיפרו את אחוזי ההישרדות (11.1 לעומת 6.8 חודשים), הישרדות ללא התקדמות המחלה PFS (6.4 לעומת 3.3 חודשים), ושיעור תגובה אובייקטיבית (31.6% לעומת 9.4%) בהשוואה לטיפול חד-תרופתי גמציטבין. רק ב20% מהחולים בניסוי זה נמצאו משקעי גידול בחלל הצפק ובאופן כללי היה להם יכולת תפקודית גבוהה יותר ואולי אפילו פרוגנוזה טובה יותר מאשר האוכלוסייה הרחבה יותר של חולים עם סרטן לבלב מתקדם. יש עניין גובר בכימותרפיה היפרתרמית (HIPEC) לטיפול בחולי סרטן עם גרורות בחלל הצפק. עם זאת, ישנו ניסיון קליני מועט בטיפול בשיטה זו סרטן הלבלב. קיימים כמה נתונים ראשוניים (N = 21) לשימוש HIPEC כטיפול מסייע לאחר כריתת גידול הלבלב הראשוני. הטוענים כי זה עשוי להפחית את שיעורי הישנות המקומית, אולם נדרשים מחקרים גדולים בהרבה. המגבלות הברורות במחקר הן גודל המחקר, ניסיון של מרכז יחיד, היעדר קבוצת ביקורת, והעובדה שאיסוף נתונים וניתוח היו רטרוספקטיביים ולא פרוספקטיביים. עם זאת, נתוני פיילוט אלה הינם משכנעים מספיק על מנת להצדיק ביצוע מחקר עתידי, אולי באמצעות ניסוי פרוספקטיבי הכולל מרכזים רבים. שמטרתו יכולה להיות פשוט לחזור על התוצאות הללו או להכליל משתנים בלתי תלויים, נניח עם או ללא היפרתרמיה, ומתן תוך-ורידי לעומת מתן תוך-צפקי של ציספלטין, כדי להגדיר טוב יותר את תרומתם של המרכיבים האישיים במשטר זה.



