Chemoradiation with hyperthermia in the treatment of head and neck cancer
International Journal of Hyperthermia, 2010 February, vol. 26:1, 21-25.
Nagraj G. Huilgol1, Sapna Gupta1 and Rajesh Dixit2
- Advanced Centre for Radiation Oncology, Dr Balabhai Nanavati Hospital, Mumbai, India
- Tata Memorial Hospital, Mumbai, India
תקציר
מטרה: ניהול הטיפול בסרטן הראש והצוואר (head and neck cancer) דורש אינטגרציה מיומנת של מספר שיטות מרובות כגון ניתוח, הקרנות, כימותרפיה והיפרתרמיה. כימורדיותרפיה (chemoradiation) יכולה להפיק תועלת מהוספתה של שיטה מוכחת כגון היפרתרמיה בהגברת ההישרדות, ההישרדות ללא-מחלה (disease-free survival) ובאיכות החיים מבלי להגביר את הסיכון לסיבוכים. מטרת מחקר רטרוספקטיבי זה הייתה להעריך את ההיתכנות והיעילות של היפרתרמיה עם כימורדיותרפיה (chemoradiation) בסרטן מתקדם של הראש והצוואר (advanced head and neck cancers).
חומרים ושיטות: בין השנים ינואר 2004 למאי 2008, 40 מטופלים עם סרטן מתקדם של הראש והצוואר הוקצו להיפרתרמיה עם כימורדיותרפיה. כל המטופלים עברו טיפולי הקרנות במכשיר טלקובלט (telecobalt machine). מינון כולל של 70 Gy ב 7 שבועות עם קיטוע קונבנציונאלי (conventional fractionation) ניתנה עם כימותרפיה שבועית של ציספלטין (cisplatin) 50 מ"ג או פקליטקסל (paclitaxel) 60 מ"ג. המטופלים עברו היפרתרמיה במכשיר גלי-רדיו (radiofrequency machine) בתדר 8.2 MHz למשך 30 דקות בטמפרטורה של 41 עד 43 מעלות צלזיוס, עם קירור מקדים (pre-cooling) של 10 דקות ל-5 מעלות צלזיוס.
תוצאות: לאף מטופל לא היו סיבוכים מסכני חיים. רק 38 מתוך 40 מטופלים היו כשירים להערכה של תגובה מיידית (immediate response) שכן, מטופל אחד נפטר במהלך הטיפול והשני לא השלים את הטיפול. התגובה המלאה (Complete response) הייתה 76.23% (29 מטופלים), ול-23.68% (9 מטופלים) הייתה תגובה חלקית (partial response). ההישרדות הכוללת (Overall survival) שהוערכה בשיטת קפלן-מאיר (Kaplan−Meir method) עמדה על 75.69% לאחר שנה אחת ו-63.08% לאחר שנתיים. לא תועדה רעילות מוגברת ברירית (mucosal) או רעילות תרמית בהשוואה לניסיון הקודם של החוקרים במחקר עם כימורדיותרפיה (chemoradiation).
מסקנה: ניתוח רטרוספקטיבי זה מדגים את ההיתכנות והיעילות של כימורדיותרפיה (chemoradiation) עם היפרתרמיה בסרטן מתקדם של הראש והצוואר. המחקר מספיק מתמרץ על מנת להתחיל בניסוי אקראי בכדי להשוות טיפול בכימורדיותרפיה (chemoradiation) עם שיטת טיפול משולשת (triple modality).
מבוא
ניהול הטיפול בסרטן מתקדם של הראש והצוואר (head and neck cancer) דורש אינטגרציה מיומנת של מספר שיטות שונות כגון הקרנות, ניתוחים, כימותרפיה והיפרתרמיה. כימורדיותרפיה (chemoradiation) התפתחה בעשור האחרון כסטנדרט הטיפולי בתת-קבוצות אנטומיות מסוימות כגון סרטן הגרון (laryngeal) וסרטן ההיפופרינקס (hypopharyngeal). Adelstein ואח'. דיווחו על שיפור בהישרדות לאחר טיפול בכימורדיותרפיה (chemoradiation) במקביל עם ציספלטין (cisplatin) על פני טיפול בקרינה בלבד. כל 225 המטופלים עם סרטן בלתי ניתן לניתוח של חלל הפה (oral cavity), אורופארינקס (oropharynx), הגרון (larynx), או היפופרינקס (hypopharyngeal) נכללו בסדרה. Bonner ואח'. במחקר שלהם על סטוקסימאב (cetuximab), מעכב גורם גדילה וסקולרי אנדותליאלי (vascular endothelial growth factor inhibitor), הראו שיפור בשליטה המקומית (local control) ובהישרדות של 3 שנים בסרטן הראש והצוואר מסוג תאי קשקש (squamous cell) שבלתי ניתנים לניתוח. כימורדיותרפיה יכולה כנראה להפיק תועלת מהוספה של שיטה מוכחת כגון היפרתרמיה בהגדלת ההישרדות, במרווח ללא מחלה (disease-free interval) או באיכות החיים.
Valdagni, הדגים יתרונות הישרדותיים מובהקים בשילוב של היפרתרמיה עם טיפולי הקרנות בסרטן הראש והצוואר. הנתונים של החוקרים שלא פורסמו, של 120 מטופלים, הראו תגובה מלאה (complete response) מרשימה של 70% מיד לאחר היפרתרמיה והקרנות. היעילות של היפרתרמיה עם קרינה הוכחה באופן חד משמעי על ידי Van der Zee ואח'. בסרטן האגן (pelvic cancers).
תרופות ציטוטוקסיות מסוימות כגון ציספלטין (cisplatin) הראו השפעות סנסטיזציה תרמיות במבחנה (in vitro) בעוד שטקסנים (taxanes) ואנתרציקלינים (anthracyclines) לא הראו שום פוטנציאל כזה. עם זאת, ההשפעה האפשרית המתווספת או מעצימה של תרופות אלה in vivo, מתעלה על מנגנונים הקשורים לשינויים תאיים בלבד. מכאן שתוצאות במבחנה (in vitro) עשויות שלא לשקף את המציאות בקליניקה. הניתוח הרטרוספקטיבי המדווח כאן נובע ממוסד ומחבר בודד. המטופלים טופלו והוערכו במהלך ארבע השנים האחרונות. זוהי ביקורת קלינית (clinical audit) ומחקר של ההיתכנות של הוספת היפרתרמיה לכימורדיותרפיה בטיפול בסרטן הראש והצוואר.
חומרים ושיטות
חולים עם סרטן הראש והצוואר עם שלבים III ו-IV טופלו בהקרנות חיצוניות רדיקליות (radical external radiotherapy), כימותרפיה שבועית והיפרתרמיה שבועית מאז 2004. המטופלים עברו אישור היסטולוגי של סרטן האפיתל (epithelial cancer), אנדוסקופיה (endoscopy), בדיקת דם של כימיה מלאה וצילום רנטגן של החזה לפני תחילת הטיפול התלת-מודאלי. לחולים עם מחלה גרורתית, צוואר קצר ושמן ומדד קרנופסקי (Karnofsky index) של פחות מ-70 לא הוצע הטיפול התלת-מודאלי. חולים עם משתנים מתערבים (confounding factors) שמנעו כימותרפיה לא טופלו בטיפול התלת-מודאלי.
טיפולי הקרנות
כל המטופלים עברו טיפולי הקרנות במכשיר (Theratron 780C, Atomic Energy of Canada Ltd, Ontario, Canada) עם אלומות פיצוי מקבילות (parallel opposed compensated beams) או אלומות מרובות (multiple beams) בהתאם הדרישה. מינון של 70 Gy תוך 7 שבועות עם קיטוע קונבנציונאלי (conventional fractionation) תוכנן עבור כל המטופלים. המטופלים טופלו 5 ימים בשבוע מיום שני עד יום שישי.
כימותרפיה
כימותרפיה שבועית ניתנה עם עירוי קצר (brief infusion) של כימותרפיה בכל יום שבת. לא ניתן טיפול קרינה ביום שבת, אך היפרתרמיה עם גלי רדיו של 8.2 MHz יושמה בתוך שעה מהטיפול בכימותרפיה. מנה של 50 מ"ג ציספלטין (cisplatin) או פקליטקסל (paclitaxel) 60 מ"ג ניתנה מדי שבוע כעירוי של 1.5 שעות עם פרה-מדיקציה (premedication) מתאימה.
היפרתרמיה
המטופלים עברו היפרתרמיה במכשיר גלי רדיו (radiofrequency machine) ב-8.2 MHz. כל המטופלים עברו קירור מקדים (pre-cooling) של 10 דקות ל-5 מעלות צלזיוס. זוג אנטנות הונחו על פני הצוואר בהנחיה באמצעות גידולים הגלויים לעין או נקודות ציון אנטומיות (anatomical landmarks). קלט (input) תדרי הרדיו (radiofrequency) הופעלו לאחר התאמת העכבה (impedance matching). ההספק השתנה בין 400 ל 800 קילוואט (kW). עלייה הדרגתית של ההספק הופסקה כאשר המטופלים התלוננו על אי נוחות או כאב. תרמומטריה פולשנית עם גישושית תרמיסטור (thermistor probe) בוצעה כאשר היה אפשרי. המטופלים קיבלו היפרתרמיה למשך 30 דקות בטמפרטורה של ב-41-43 מעלות צלזיוס, לאחר קירור מקדים למשך 10 דקות. המטופלים הוערכו פעמיים בשבוע על מנת להעריך רעילות אקוטית ותגובה. למטופלים שפיתחו נויטרופניה ניתנו גורמים מעוררי גידול מושבות (colony-stimulating factor), אולם המשיכו בפרוטוקול. עם זאת, היפרתרמיה הושהתה במידה והמטופלים פיתחו כוויות תרמיות (thermal burns) בדרגה 2 ומעלה.
זהו מחקר של מוסד בודד שנותח באופן רטרוספקטיבי.
לאחר אי הכללת כפילויות, המאמרים נסרקו על סמך הכותרות והתקצירים שלהם. נושאים שאינם קשורים לסרטן הראש והצוואר (HNCs), מחקרים תרמו-רדיוביולוגיים (thermoradiobiological) במבחנה (in vitro), מאמרים טכניים על מכשור היפרתרמיה, מינון תרמי, סקירות, דיווחי מקרה, שימוש בכימותרפיה במקביל עם הקרנות ו/או היפרתרמיה, שימוש בברכיתרפיה אינטרסטיציאלית (interstitial brachytherapy), ננוטכנולוגיה (nanotechnology), טיפולים חוזרים ומאמרים שאינם באנגלית לא נכללו כמפורט באיור 1. מאמרים שעודכנו בפרסום מאוחר יותר על ידי אותם המחברים ואלה עם קבוצות מטופלים מעורבות שבהן התוצאות של סרטן הראש והצוואר (HNCs) לא ניתנו בנפרד, הושמטו.
מטופלים והערכת התוצאות
התגובה המיידית (Immediate response) נותחה כתגובה מלאה (complete), תגובה חלקית (partial) או ללא תגובה, בהתאם להנחיות ארגון הבריאות העולמי (WHO). המטופלים הוערכו באופן תקופתי לצורך הערכת מצב המחלה ואת הרעילות במרווח של 3 חודשים בשנה הראשונה ובמרווח של 6 חודשים בשנים שלאחר מכן. הרעילות בהיפרתרמיה הוערכה על ידי כוויות בדרגות בין 1 ל-4. דרגה 1 – כוויה שטחית עם עובי חלקי, דרגה 2 – כוויה עמוקה עם עובי חלקי, דרגה 3 – כוויה בעובי מלא, דרגה 4 – נמק של הרקמות הרכות. מטופלים שנפטרו ואלו שאבדו למעקב צונזרו לצורך ניתוח ההישרדות לאחר מכן. בוצע ניתוח ההישרדות של קפלן-מאייר (Kaplan–Meier survival analysis).
תוצאות
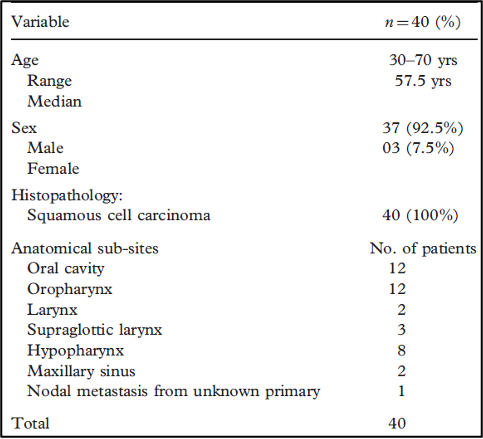
ארבעים מטופלים עם סרטן הראש והצוואר טופלו במהלך ארבע השנים האחרונות בטיפול קרינתי-כימותרפי משולב והיפרתרמיה. טבלה 1 מציגה את הפרופיל הקליני עם אתרי משנה אנטומיים של קבוצה זו. מרבית המטופלים סבלו מסרטן חלל הפה ומסרטן האורופרינקס (oropharyngeal). רק לשני מטופלים היה נגע בדירוג T2N0M0, בעוד שלשאר המטופלים היו נגעים בדירוג T3-T4 וגרורות בבלוטות הלימפה בצוואר (metastatic neck nodes) בדירוג N0-N3. טבלה 2 מציגה ריבוד בהתאם לדירוג TMN (AJCC).
להלן טבלה 1: הפרופיל הקליני
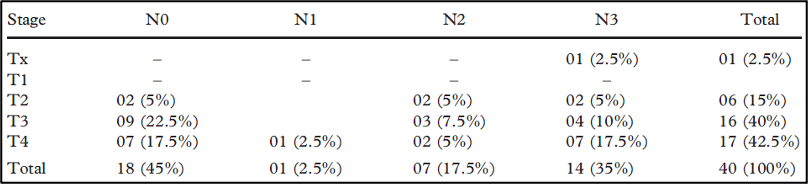
להלן טבלה 2: ריבוד בהתאם לדירוג TMN (AJCC)
רק 38 מטופלים היו כשירים להערכה של התגובה המיידית מכיוון שמטופל אחד נפטר במהלך הטיפול והשני לא השלים את הטיפול. המוות לא היה קשור לאף שיטת טיפול. מינון הקרינה הכולל שניתן נע בין 60 Gy ל-70 Gy עם מינון ממוצע של 66.23 Gy (סטיית תקן-4.079).
המטופלים קיבלו היפרתרמיה למשך 30 דקות בטמפרטורה של 41-43 מעלות צלזיוס לאחר קירור מקדים של 10 דקות. התרמומטריה בוצעה ב-23 מטופלים שסבלו מגרורות בבלוטות הלימפה. הטמפרטורה המקסימלית מעולם לא עלתה על 43 מעלות צלזיוס באף אחד מהמטופלים. הטמפרטורה הממוצעת היא 42.4 מעלות צלזיוס לאחר ניכוי חריגה אחת ב-39 מעלות צלזיוס.
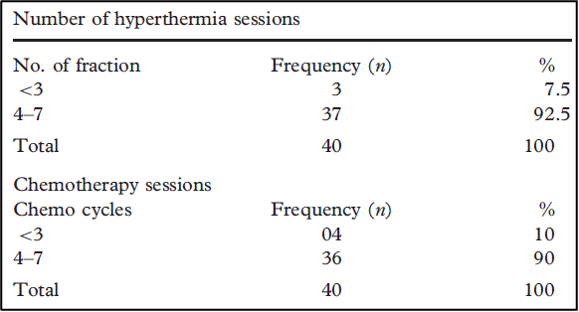
טבלה 3 מציגה את מספר מפגשי הטיפול של היפרתרמיה ומספר מחזורי הכימותרפיה שניתנו לכל המטופלים. הרוב המוחלט של 37 מטופלים קיבלו יותר מארבעה מפגשי טיפול בהיפרתרמיה. באופן דומה, 36 מטופלים קיבלו יותר משלושה מחזורים (4-7) של כימותרפיה. אלה שקיבלו פחות מ-3 מחזורים של כימותרפיה עשו זאת בגלל רעילות הקשורה לכימותרפיה כמו בחילות והקאות. מספר שווה של מטופלים קיבלו ציספלטין (cisplatin) ופקליטקסל (paclitaxel). בעוד שחולה אחד שנפטר, מטופל אחד קיבל טיפול חלקי בקבוצת הפקליטקסל (paclitaxel group). המעקב נע בין 4 ל-68 חודשים עם משך חציוני של 9 חודשים.
להלן טבלה 3: פרטים על תדירות מפגשי הטיפול של היפרתרמיה וכימותרפיה עם טיפול בקרינה ב-40 מטופלים עם סרטן הראש והצוואר.
להלן טבלה 4: תגובה ראשונית של מטופלים מבחינה תרופתית
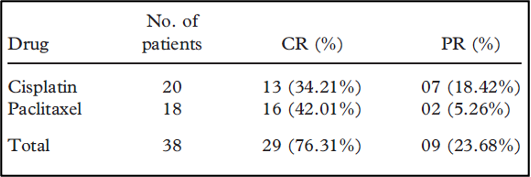
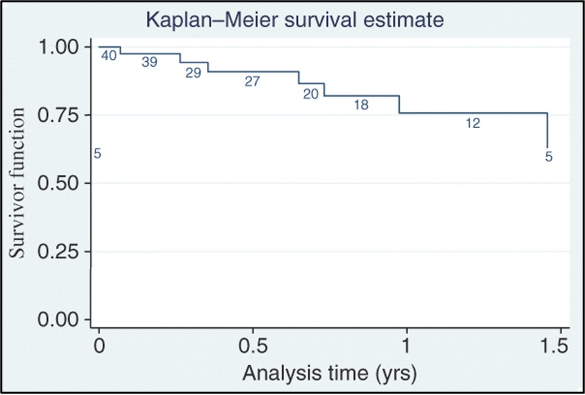
מתוך 38 מטופלים, תגובה מלאה (CR) תועדה ב-29 מטופלים (76.32%) ולתשעה מטופלים (23.68%) הייתה תגובה חלקית (PR). בנוגע ל-29 המטופלים עם תגובה מלאה (CR), 13 (34%) טופלו בציספלטין (cisplatin), ו-16 (42%) עם פקליטקסל (paclitaxel) (P: 0.479). מתוך תשעת המטופלים עם תגובה חלקית (PR), שבעה (18%) היו בקבוצת ציספלטין ושניים (5%) היו בקבוצת הפקליטקסל. מטופל אחד נפטר ומטופל אחד קיבל טיפול חלקי בקבוצת הפקליטקסל. איור 1 מציג את עקומת ההישרדות של קפלן-מאייר (Kaplan-Meier survival curve). ההישרדות הכוללת (OS) בשיטת קפלן-מאיר הייתה 75.69% לאחר שנה (95% confidence interval (CI) 51.88–88.85) ולאחר שנתיים היא עמדה על 63.08 (95%CI 30.98–83.43). מתוך 40 (92.5%) מטופלים, 37 קיבלו ארבע או יותר (4-7) מפגשי טיפול בהיפרתרמיה, בעוד ש-36 מתוך 40 (90%) מטופלים קיבלו ארבעה או יותר (4-7) מפגשי טיפול כימותרפיים. לפיכך, ניתן לשער כי הרוב המוחלט של המטופלים עמדו בפרוטוקול הטיפול התלת-מודאלי. שבעה מטופלים אבדו למעקב במרווחי זמן שונים.
להלן איור 1: הערכת ההישרדות של קפלן-מאייר (Kaplan-Meier survival) לאחר טיפול בכימורדיותרפיה והיפרתרמיה
לא תועדה רעילות מוגברת ברירית (mucosal) או רעילות תרמית בהשוואה לניסיון הקודם של החוקרים במחקר עם כימורדיותרפיה (chemoradiation). שני מטופלים סבלו מכוויות בדרגה 1 באזור קטן שתואם לקצה האנטנות. הטיפול לא הופסק אצל אף מטופל בעקבות כוויות תרמיות. הם החלימו בסופו של דבר עם שימוש בנאדוקין (nadoxin), אנטיביוטיקה ותרופות משככות כאבים.
בהתבסס על קריטריוני המחקר שהוגדרו מראש, איכות המחקר הוערכה בהתאם להנחיות של PRISMA. הוערכו כל הגורמים האפשריים הקשורים למאפייני המטופלים ולפרמטרים של הטיפול שיכולים להשפיע על התוצאה. רק המחקרים שדיווחו על תגובה מלאה (CR) בעבור החולים שטופלו בהקרנות ובהיפרתרמיה, או כאשר ניתן היה לחשב בהם תגובה מלאה (CR) מהנתונים המוצגים במאמרים נלקחו בחשבון.
דיון
כימורדיותרפיה התפתחה כסטנדרט הטיפולי של ניהול הטיפול בסרטן הראש והצוואר, כמו גם בסרטן הריאות וכן בסרטן צוואר הרחם. Adelstein ואח'. הדגימו יתרון הישרדותי באותם מטופלים עם סרטן הראש והצוואר בלתי ניתן לכריתה שקיבלו טיפול קרינה שיגרתי (conventional radiation) וציספלטין (cisplatin) על פני מטופלים שטופלו בהקרנות בלבד. ההישרדות השתפרה מ-27% ל-37% לאחר 3 שנים. רעילות מוגברת נצפתה עקב כימותרפיה. כימורדיותרפיה הוכחה כמשפרת את השליטה המקומית-אזורית (loco-regional control) ואת ההישרדות הכוללת (OS) באתרי משנה רבים של קרצינומה של תאי הקשקש (squamous cell carcinoma) בראש ובצוואר. ההישרדות הכוללת (OS) שדווחה על ידי Bonner ואח’. היא רק 55% לאחר 3 שנים עם סטוקסימאב (cetuximab), ו-Brizel ואח’. הוכיחו גם הם הישרדות כוללת (OS) דומה של 55% לאחר 3 שנים לאחר טיפול קרינתי-כימותרפי משולב (concurrent chemoradiation). קיים מקום וצורך דחוף בשיפור נוסף בהישרדות.
טיפול בכימורדיותרפיה מוביל להגברת רעילות אקוטית של הרירית והעור. כמו כן, הולכות ומצטברות עדויות לרעילות כרונית מוגברת. מלבד זאת, שתי מטא-אנליזות שפורסמו לאחרונה הטילו ספק בהשפעה של טיפול הכימורדיותרפיה על גידולים בשלבים מתקדמים.
מספר רב של גידולים שאינם רגישים לתרופות ציטוטוקסיות נותרים חשוכי מרפא גם לאחר טיפול בכימורדיותרפיה; סיבה נוספת לגידולים עמידים אלה היא היפוקסיה של הרקמות. חום הוא רדיוסנסטיזטור יעיל לקרינה. גם התאים ההיפוקסיים פגיעים למוות תאי בעקבות היפרתרמיה, שלא כמו לאחר הקרנות וכימותרפיה. Martin Franckena ואח'. הציעו כי יהיה מועיל יותר להוסיף היפרתרמיה להקרנות מאשר כימותרפיה להקרנות בסרטן בשלבים מתקדמים יותר.
כישלון לשפר את ההישרדות עוד יותר יכול להיות בגלל אכלוס מחדש בלתי נשלט של שיבוטים עמידים (resistant clones) של תאים, היפוקסיה, והעברת תרופות ירודה בעקבות פרפוזית דם לקויה. היפרתרמיה יכולה להתגבר על היפוקסיה, להגביר את הפרפוזיה בטמפרטורות נמוכות יותר ולפעול על אותם התאים אשר עמידים לקרינה. זוהי, אם כן, סיבת הבסיס להוספת היפרתרמיה לכימורדיותרפיה. שיפור תרמי לאחר מתן כימותרפיה עשוי לנבוע מספיגה מוגברת של התרופות, עלייה בפרפוזיה, הגברה של הנזק לדנ"א או עיכוב של תיקון הנזק לדנ"א, ו/או זה עשוי להיות שילוב של מנגנוני הפעולה שלעיל. טיפול בכימורדיותרפיה עם היפרתרמיה הוא תחום הדורש חקירה ובדיקה בקליניקה. לא כל התרופות הראו שיפור תרמי במבחנה (in vitro). חומרים מאלקלים (Alkylating agents), אנלוגים של פלטינום (platinum analogues), בלאומיצין (bleomycin) ומיטומיצין (mitomycin), נחשבים בעלי ערך. בעוד שאלקלואידים של vinca, טקסנים (taxanes), טופוטקאן (topotecan), 5-FU ומתוטרקסט (methotrexate) לא הדגימו שביעות רצון תרמית מספקת. Arcangeli ואח’. הדגימו יתרון בשילוב של אדריאמיצין (adriamycin) ובלאומיצין (bleomycin) עם היפרתרמיה, כאשר סך של 29 מטופלים עם סרטן הראש והצוואר עם בלוטות לימפה הדגימו תוצאה חיובית. מחקר זה הראה את היעילות המוגברת של אדריאמיצין (adriamycin) ובלאומיצין (bleomycin) בשילוב עם היפרתרמיה מקומית (local hyperthermia) בגרורות בבלוטות הלימפה בצוואר מסרטן הראש והצוואר. Kohno ואח’. הדגימו גם את היעילות בשילוב של בלאומיצין (bleomycin) ומיטומיצין (mitomycin) עם היפרתרמיה בממאירויות במחקר אקראי שכלל 65 מטופלים.
גישה תלת-מודאלית לטיפול בסרטן הראש והצוואר פורסמה קודם לכן, על ידי Amichetti בקבוצה קטנה של מטופלים. מחקר זה מראה את ההיתכנות של יישום טיפול תלת-מודאלי בסרטן הראש והצוואר. לא נצפו רעילויות מונעות. תגובה ראשונית במטופלים שטופלו בפקליטקסל (paclitaxel) וציספלטין (cisplatin) היא תצפית מעניינת, שכן טקסנים (taxanes) לא הדגימו סנסטיזציה תרמית במבחנה (sensitisation in vitro). אבל Anna Cividalli ואח’. הוכיחו במחקר שלהם כי היפרתרמיה הגבירה את האפקטיביות של פקליטקסל (paclitaxel) in vivo וההערכה, במונחים של מרפא (cure) מראה על יחס שיפור גבוה מאוד. ההשערה היא כי פרפוזיה מוגברת ככל הנראה הובילה לריכוז תאי גבוה יותר עם השפעות קטלניות. ציספלטין (cisplatin) ופקליטקסל (paclitaxel) הן חלק מהמולקולות המשמשות בטיפול הכימורדיותרפיה של סרטן הראש והצוואר. הוכח כי ציספלטין (cisplatin) בעל רגישות תרמית, בעוד שההשפעות על פקליטקסל (paclitaxel) כבעל רגישות תרמי הן דו-משמעיות. ההנחה היא שהתוספת של היפרתרמיה לטיפול בכימורדיותרפיה עם פקליטקסל (paclitaxel) או ציספלטין (cisplatin) מראה תגובה מצטברת.
מחקר זה מתעד את ההיתכנות והיעילות של גישה תלת-מודאלית של טיפול עם פקליטקסל, ציספלטין, היפרתרמיה והקרנות. מעקב ארוך טווח ומחקרים אקראיים יסייעו להעריך את התועלת המדויקת של טיפול בגישה תלת-מודאלית על פני טיפול בכימורדיותרפיה בלבד.
מסקנות
ניתוח רטרוספקטיבי זה מדגים את ההיתכנות של טיפול בכימורדיותרפיה עם היפרתרמיה בסרטן מתקדם של הראש והצוואר. סרטן הראש והצוואר עם מסת גידול (tumour burden) גבוהה מאוד יש סיכויי הישרדות עגומים. מחקר זה מעודד מספיק על מנת להתחיל בניסוי אקראי בכדי להשוות בין כימורדיותרפיה לבין כימו-היפרתרמיה והקרנות.



